- Ирина, чем, по сути, являются генерические лекарственные средства?
- История любого лекарственного средства начинается с этапа разработки. Оно создается на основе новой, впервые синтезированной или полученной из природного сырья субстанции. Так как это новое активное вещество, оно проходит полный цикл доклинических и клинических исследований и защищается патентом на определенный срок (в среднем на 15-20 лет). Патентная защита дает возможность монопольной торговли на рынке и позволяет производителю-оригинатору компенсировать затраты на разработку и исследования. Когда срок патентной защиты заканчивается, данное инновационное лекарство могут производить другие компании. Именно так и появляются генерики. По большому счету, это просто следующая фаза жизненного цикла оригинального препарата. Важно, что в отношении генериков не нужно проводить доклинические и клинические исследования в полном объеме. Достаточно доказать эквивалентность данного генерика оригинальному препарату: фармацевтическую (идентичность состава по содержанию активного вещества, примесей оригинальному препарату), и/или биологическую (фармакокинетическую) эквивалентность, т.е. сходство биодоступности (скорости и степени всасывания) действующего вещества. О биоэквивалентности судят, сравнивая параметры скорости попадания препарата в кровоток, распределения его в нем и выведения из живого организма, что наглядно демонстрируется сравнением площади под кривой «концентрация - время» при введении генерика и оригинального препарата здоровым добровольцам. Эта кривая по установленным параметрам биоэквивалентности должна находиться в пределах 80–125% от кривой для оригинального препаратаб что отражает допустимую вариабельность поведения лекарственного препарата в организме. Но сожержание действующего вещества в сериях испытуемого и референтного препарата не должно отличаться более, чем на 5%.
Гарантией постоянного соответствия параметров качества генериков, как и любых лекарственных средств, той спецификации, что была заявлена при государственной регистрации, служит сертификация GMP.
Совокупность этих условий и применение лекарственного средства в соответствии с инструкцией позволяет предполагать, что генерик терапевтически эквивалентен оригинальному лекарству. Однако не для всех препаратов можно провести исследование на биоэквивалентность. Примером могут являться инъекционные лекарственные средства. Они вводятся непосредственно в кровоток и, естественно, все 100% действующего вещества сразу достигают системного кровообращения. Для таких препаратов определяют терапевтическую биоэквивалентность по.
Как видно, разработка генериков - более простой процесс, чем первоначальное создание оригинальных препаратов. Именно этим и объясняется их меньшая стоимость, так как не нужно закладывать риски неуспеха разработки. Но никах не худшими условиями производства или материалов. Благодаря генерикам, терапия инновационным лекарством, которая ранее стоила очень дорого, становится доступной для всех, кто в ней нуждается. Разве не это самое главное?
Но на генериках жизненный цикл лекарства не останавливается и далее переходит в категорию, так называемых, хорошо изученных (традиционных) препаратов. В соответствии с текущим регулированием, для этого достаточно 10 лет задокументированного успешного использования в реальной клинической практике. Примером традиционных лекарственных средств являются ацетилсалициловая кислота или парацетамол. Ведь, когда мы покупаем их в аптеке, нам даже в голову не приходит спрашивать оригинальный это или генерический препарат. Именно такими цивилизованными должны быть отношения на фармацевтическом рынке, без антагонизма и нездоровой конкуренции в виде распространения МИФОВ о том, что оригинальный препарат всегда лучше просто потому что он был первым.
- Насколько обосновано это утверждение?
- Судите сами, прежде, чем появится генерик на рынке проходит в среднем 15-20 лет. С точки зрения развития науки - это огромный срок. Все мы знаем насколько интенсивно она развивается, особенно в последнее время. Появляются новые технологии синтеза веществ, очистки от примесей, стабилизации и т.д. Поэтому генерик иногда может даже превосходить оригинальный препарат по своим параметрам фармацевтического качества, например, более длительный срок годности. Однозначно данное утверждение – это МИФ.
- Может ли производитель продлить жизненный цикл давно присутствующего на рынке препарата?
- Конечно, производитель может изменить качественные характеристики препарата и, тем самым, улучшить его терапевтическую эффективность. Такие препараты носят название лекарственных средств с добавленной ценностью. К примеру, производитель может значительно улучшить клинические исходы, изменив лекарственную форму (таблетку на таблетку растворимую или таблетку с пролонгированным высвобождением действующего вещества), или провести исследования и расширить показания применения препарата, добавив новую терапевтическую цель. Примеров таких можно привести очень много. Причем сделать это может как оригинальный, так и генерический производитель.
- Оригинальные препараты иногда сравнивают с автомобилями представительского класса. Этично ли такое сравнение?
- Однозначно - нет. Ведь обладание автомобилем представительского класса, это не жизненная необходимость, а скорее стремление удовлетворить свои эмоциональные потребности, которые связаны с желанием продемонстрировать роскошь, принадлежность к определенному социальному классу и т.д. Когда речь идет о здоровье, вопрос не стоит купить или не купить, лечиться или не лечиться. Пациент нуждается в терапии, и он должен ее получить. Здесь нет места эмоциям, завязанным на престиже или особенном статусе. Здесь нужно руководствоваться только рациональным выбором. Иначе будет очень сложно обеспечить социальную справедливость и конституционные гарантии права каждого гражданина на здоровье.
Главное в данном случае - это функционал. Безусловно, комфортно доехать из точки «А» в точку «Б» на автомобиле Mercedes представительского класса – это престижно. Но, гуманно ли, если проедет один, а все остальные пойдут пешком. Именно генерики позволяют проехать весь путь всем, а не отдельным членам общества. И, если они столь же эффективны и безопасны, как оригинальные лекарственные средства, то вопрос престижа здесь просто неуместен. В принципе, мы должны избавляться от исторических стигм, которые десятилетиями навязывались потребителям и являются в большей степени мифами.
- Заявления такого рода всегда ставят под сомнение силу регуляторного поля в стране.
- Да, но это очередной МИФ. Фармацевтическая отрасль отличается самым сильным и жестким регулированием. Вывести препарат на рынок определенной страны, в том числе Казахстана, весьма непросто. Для этого необходимо пройти всестороннюю длительную экспертизу в Национальном центре экспертизы лекарственных средств, изделий медицинского назначения МЗ РК. Сегодня мы можем с уверенностью говорить о высоком научно-техническом и профессиональном уровне казахстанского экспертного органа, который в состоянии закрыть доступ на рынок для некачественных лекарственных средств.
- Ирина, довольно часто звучит мнение, что генерики предназначены для жителей бедных стран, а в развитых государствах применяются только оригинальные препараты. Так ли это?
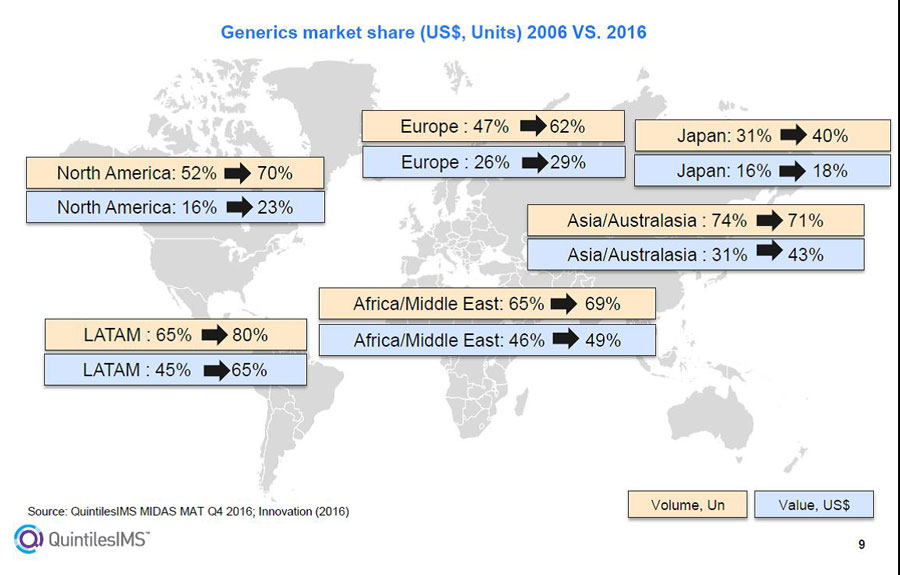
- Это есть ни что иное, как еще один МИФ. Факты свидетельствуют об обратном. В соответствии с данными лидирующей международной консалтинговой компании IQVIA, лидером по потреблению генериков являются страны Северной Америки и Европы. Общеизвестно, что лидером мирового фармацевтического рынка являются США. Это самый большой по емкости и самый престижный рынок. Именно на него в первую очередь все фармацевтические производители стремятся вывести инновационные дорогостоящие продукты и технологии. И в тоже время именно в этой стране выписывается самое большое количество рецептов на генерики. Так, по данным компании IQVIA, потребление генериков в упаковках в странах Северной Америки с 2006 по 2016 год увеличилось с 52 до 70% (рисунок). Причем, затраты на них были не столь значительными и выросли с 16 до 23%. Это яркое свидетельство социальной значимости генериков. Только представьте, на 70% использованных лекарств были потрачено лишь 23% ресурсов.
Рисунок
Доля генериков в стоимостном и натуральном выражении в разных регионах мира в 2006-2016 годах
- Нередко звучит вопрос: почему отечественная фармацевтическая промышленность ориентирована на генерики? Что вы скажете по этому поводу?
- Оглянитесь на 15 лет назад, когда отечественные фармацевтические предприятия выпускали весьма ограниченный ассортимент продукции. При этом не было обязательной сертификации по стандартам GMP. Сегодня в стране функционируют крупные заводы. За сравнительно небольшой промежуток времени, благодаря поддержке государства, они были модернизованы или вообще отстроены с нуля, оснащены современным оборудованием, был обучен персонал и, самое главное, налажен выпуск широкого ассортимента современных качественных генериков, востребованных в здравоохранении. Ничего не бывает сразу. Все образуется постепенно. К примеру, сейчас в компании SANTO функционирует подразделение R&D, которое занимается научными разработками и исследованиями в области фармацевтики.
Говоря о качестве отечественных препаратов, необходимо отметить, что они также проходят тщательную оценку на этапе государственной регистрации, в том числе лабораторные испытания и клинические исследования, а наши производственные площадки регулярно инспектируются на соответствие стандартам GMP. Вообще, компания SANTO, как лидер казахстанской фармацевтической индустрии ориентируется на производство жизненно важных необходимых лекарственных средств. В Казахстане нет такого списка, но, если вы посмотрите соответствующий список ВОЗ, вы увидите максимальное совпадение, но с учетом эпидемиологической ситуации в нашей стране. Мы стремимся удовлетворить основные потребности системы здравоохранения. Именно в этом мы видим свою социальную роль.
Ольга Баимбетова












