ГЛАВНЫЕ НОВОСТИ
Мастер-классы

В Алматы впервые в истории казахстанской медицины состоялся международный мастер-класс по проведению ранней витрэктомии у недоношенных детей — высокотехнологичной операции, которая даёт младенцам шанс не потерять зрение навсегда.
Это были не просто четыре дня хирургической практики — это были четыре дня, в которые в буквальном смысле спасались глаза, свет, будущее. Потому что потеря зрения в младенческом возрасте — это не просто медицинский диагноз. Это — потеря мира, цветов, лиц матери, прикосновений света, уверенности в движении, возможности учиться, играть, мечтать. Слепота — тишина, в которую может провалиться вся жизнь. Но если успеть вовремя — эту тишину можно остановить.
Мастер-класс прошёл на базе Центра детской неотложной медицинской помощи (г. Алматы) при участии доктора Нихила Пала — всемирно признанного индийского офтальмохирурга, специализирующегося на лечении тяжелейших форм ретинопатии недоношенных. За четыре дня команда врачей под его руководством провела 20 операций для 14 детей из 12 регионов Казахстана. Самому младшему пациенту — всего 2,5 месяца.
Центральной темой стал один из самых сложных и пугающих диагнозов детской офтальмологии — ретинопатия недоношенных (РН). Это заболевание сетчатки является одной из ведущих причин слепоты у новорождённых во всём мире. В Казахстане ежегодно появляется на свет более 22 000 недоношенных детей, и около 4 000 из них — в группе риска по РН.
«В последние годы ретинопатия стала настоящей эпидемией младенческой слепоты в Казахстане. Это болезнь, где счёт идёт не на дни, а на часы. Если промедлить — ребёнок может никогда не увидеть лица своей мамы», — говорит Асель Шарипова, ведущий детский офтальмохирург страны.
За последние 10 лет в Казахстане достигнут серьёзный прогресс: внедрены протоколы ранней диагностики, обучено более 40 офтальмологов, созданы региональные команды. Но до сих пор в случае тяжёлых, терминальных стадий детям приходилось ехать за границу — ведь сложнейшие витрэктомии не проводились на территории страны.
Фонд "Добровольное общество Милосердие" только за последние два года направил 166 детей на операции за рубеж — ради шанса хотя бы частично сохранить зрение. Ведь иногда даже 10% — это уже не тьма, это возможность ориентироваться, читать, улыбаться в ответ.
Теперь, благодаря мастер-классу, такая помощь стала доступна в Казахстане. Это означает не только технологический прорыв, но и новую эру в помощи самым маленьким пациентам — когда их лечение не зависит от границ.
Особую роль в этом прорыве сыграло оснащение операционного блока Центра детской неотложной медицинской помощи, где проводились операции. Благодаря поддержке фонда «Аяла», здесь появилось современное оборудование, в том числе для витреоретинальной хирургии, — необходимое условие для проведения столь сложных вмешательств. Это пример того, как объединение усилий разных фондов помогает создавать настоящие системы спасения.
Важно отметить, что в рамках мастер-класса повышение квалификации прошли 10 казахстанских врачей из Астаны, Шымкента и Алматы. Это позволит в перспективе сформировать устойчивую профессиональную базу и расширить возможности высокотехнологичной офтальмохирургии внутри страны — чтобы подобная помощь была доступна здесь, дома, без необходимости выезда за границу.
Мероприятие было организовано фондом «Добровольное общество Милосердие» при поддержке фонда «Samruk-Kazyna Trust».
«Это событие — не про хирургию. Оно про свет, который останется с ребёнком на всю жизнь. Это про возможность увидеть свою маму, впервые улыбнуться ей в ответ, увидеть небо, книги, людей, мир», — подчёркивают организаторы.
Кроме операций, специалисты обсудили вопросы развития системы офтальмологической помощи, обучения казахстанских врачей, а также перспективы международного сотрудничества в области детской офтальмологии и медицинского туризма.
Сегодня Казахстан сделал шаг не просто к технологическому суверенитету. Он сделал шаг к тому, чтобы каждому ребёнку в этой стране был дан шанс на зрение, на детство, на свет.
События

В РК начинается пилотный проект по регистрации ЛС и МИ по принципу «единого окна». Приказ утвержден!
30 апреля 2025 года состоялось официальное опубликование совместного приказа Министра здравоохранения Республики Казахстан от 22 апреля 2025 года №40 и Министра цифрового развития, инноваций и аэрокосмической промышленности Республики Казахстан от 22 апреля 2025 года №169/НҚ «О проведении пилотного проекта по государственной регистрации лекарственных средств и медицинских изделий по принципу «единого окна».
Этот исторический документ положил начало беспрецедентному пилотному проекту, направленному на упрощение процесса вывода препаратов на рынок.
Содержание документа структурировано следующим образом:
Глава 1. Общие положения, закладывающие фундамент для понимания целей и задач проекта.
Глава 2. Порядок оказания композитной государственной услуги «Регистрация лекарственных средств и медицинских изделий по принципу «единого окна», детально описывающий процедуру взаимодействия заявителей с государственными органами.
Глава 3. Порядок проведения экспертизы, регистрации, перерегистрации, внесения изменений в регистрационное досье лекарственного средства или медицинского изделия, регистрация цены и внесения изменения в цену производителя лекарственного средства или медицинского изделия, формирования предельных цен на лекарственные средства, определяющий алгоритм экспертной оценки, регистрации и контроля цен на лекарственные средства.
Глава 4. Порядок проведения экспертизы, регистрации, перерегистрации, внесения изменений в регистрационное досье медицинского изделия и регистрации, внесение изменения цены производителя, устанавливающий аналогичный порядок для медицинских изделий.
Глава 5. Правила формирования Казахстанского национального лекарственного формуляра, регламентирующие процесс создания и ведения национального перечня лекарственных средств.
Приказ объединяет 12 НПА, регламентирующих экспертизу, регистрацию и дальнейшие процедуры, необходимые для вывода лекарственных средств и медицинских изделий на рынок.
Он вводится в действие со дня его первого официального опубликования и действует до 1 июля 2025 года.
Все о лекарствах

В Астане 23-26 апреля 2025 года прошла IV Международная научно-практическая конференция по оценке технологий здравоохранения. В рамках мероприятия ведущие эксперты, представители государственных органов, фармацевтических компаний, производителей медицинских технологий, исследовательских организаций и медицинского сообщества обсудили широчайший спектр вопросов по дальнейшему формированию и развитию системы здравоохранения Казахстана и региона. В рамках конференции Президент Ассоциации поддержки и развития фармацевтической деятельности РК Марина Дурманова озвучила доклад, посвященный вопросам доступности лекарственных средств в нашей стране.
М.И. Дурманова отметила, что доступность лекарственных средств является важнейшим аспектом здравоохранения и благополучия населения.
Доступность бывает экономической, когда высокая стоимость лекарств может стать препятствием для их приобретения. Решается данная проблема введением медицинского страхования, которое должно покрывать большую часть цены или полную стоимость препарата, а также льготами для особых категорий больных социально-важными и хроническими заболеваниями. Кроме того в некоторых странах могут выделяться государственные субсидии и финансовая поддержка аптек и медицинских учреждений в сельских районах, что помогает увеличить возможность приобретения необходимых медикаментов. Для повышения экономической доступности также создаются механизмы регулирования цен и внедряются механизмы поддержки доступных лекарственных средств.
- Доступность также может быть физической и она, в свою очередь, зависит:
- ПРЕЖДЕ ВСЕГО ОТ НАЛИЧИЯ ПРЕПАРАТОВ НА РЫНКЕ, Т.Е. ИХ ФИЗИЧЕСКОГО ПРИСУТСТВИЯ В СТРАНЕ;
- от географического расположения аптек и медицинских учреждений - важно, чтобы аптеки находились в шаговой доступности для большинства населения, особенно в сельских и удаленных районах;
- от эффективной логистики и снабжения - надежные цепочки поставок гарантируют своевременное и бесперебойное поступление медикаментов в аптеки и больницы. Кроме того, для обеспечения физической доступности лекарств важно избегать сбоев в поставках, так как они могут повлиять на здоровье пациентов.
Конечно, с учетом сегодняшних возможностей, когда препарат можно заказать через интернет из другой страны и его привезут в течение двух-трех дней, проблема физической доступности может быть частично решена. Я подчеркиваю – ЧАСТИЧНО. Потому что препарат может понадобиться ЗДЕСЬ И СЕЙЧАС и иногда от этого зависит жизнь пациента. Кроме того, не нужно забывать, что при приобретении препарата через всемирную паутину высоки риски покупки фальсификата. Результат – в лучшем случае нулевая эффективность, а также напрасно потраченные деньги и время. Более того, эти препараты идут мимо выстоянной государством системы регистрации, оценки безопасности и качества, фармаконадзора. Именно эта система гарантирует пациенту получение препарата, установленного качества, эффективности и безопасности.
Что же влияет на физическую доступность:
- препарат должен быть зарегистрирован на территории страны и обращаться на рынке;
- наличие благоприятных регуляторных условий для выхода и присутствия на рынке препаратов;
- наличие понятного и стабильного законодательства;
- отсутствие барьеров (таких как: ценовое регулирование в розничном сегменте, введение НДС, регистрация по правилам ЕАЭС без сохранения национальной процедуры, любые задержки в процедуре ввода препарата на рынок).
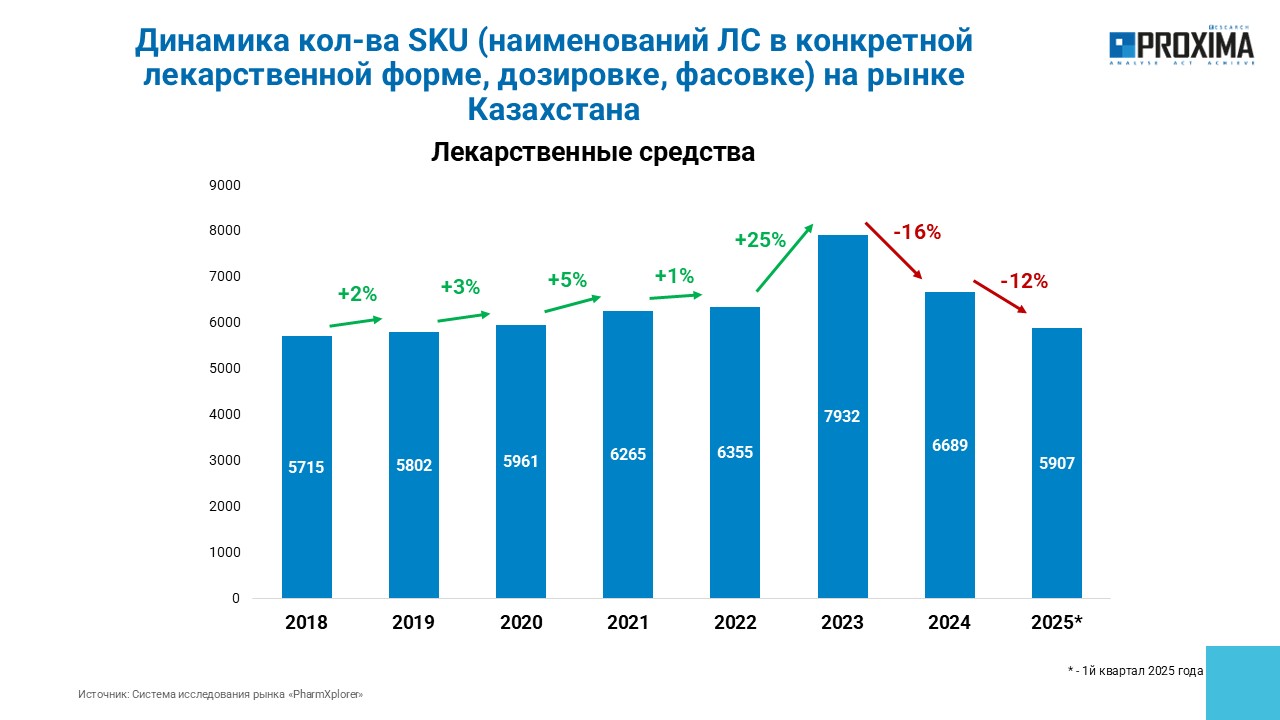
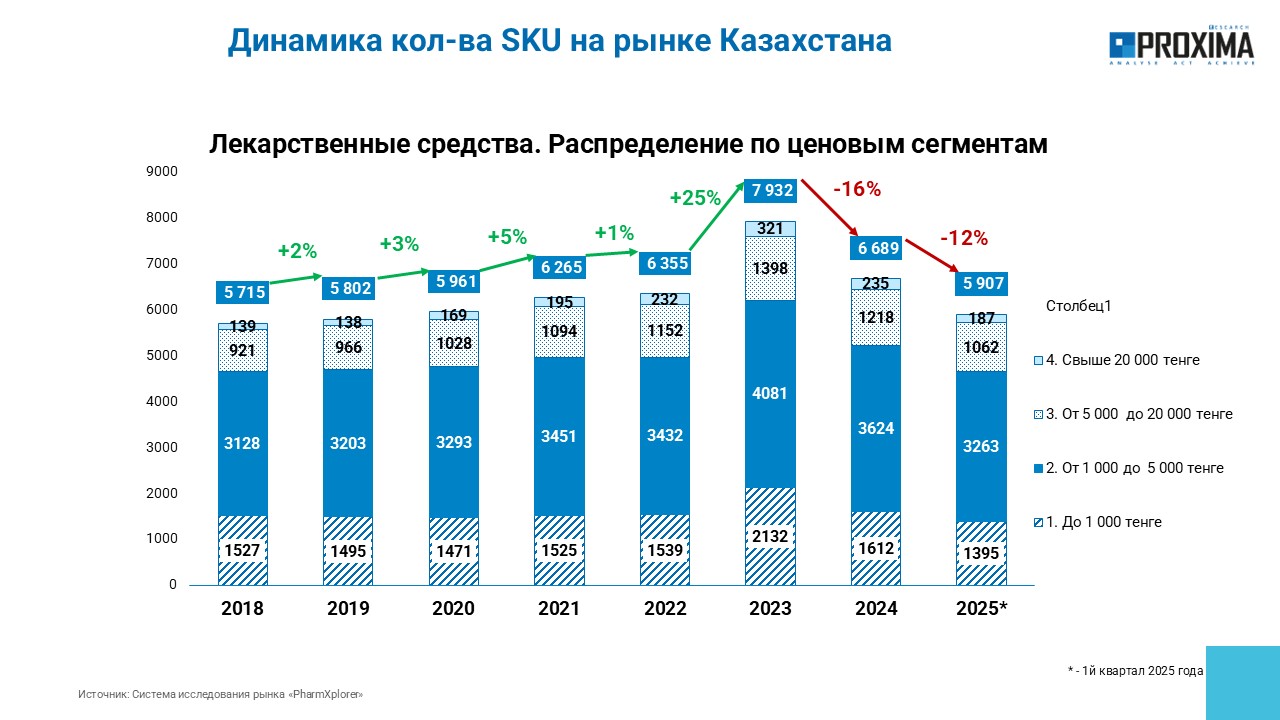
В последние годы государство предпринимает многочисленные шаги, которые увеличивают финансовую нагрузку на предприятия фармацевтической отрасли. Для того, чтобы показать, как в зависимости от введения этих норм меняется привлекательность казахстанского фармацевтического рынка для производителей лекарств, мы решили проанализировать динамику количества наименований лекарств, реально присутствующих на рынке. Сразу отмечу, что факт присутствия препарата в Государственном реестре лекарственных средств и медицинских изделий РК не говорит о том, что он продается в аптеках. Поэтому для анализа мы взяли именно данные реального рынка, а в дополнение посмотрели еще и сокращение наименований лекарств по ценовым категориям.
Итак, согласно данным PROXIMA Research, количество наименований лекарств, представленных на рынке, уменьшилось на 25,5% с 7932 в 2023 году до 5907 в настоящее время. Как отметила М. Дурманова, эта цифра очень серьезная. Но еще более впечатляет отток дешевых лекарств с рынка. Так, количество наименований препаратов с ценой до 1 000 тенге сократилось на 34,5%. Что это означает? Это означает, что некоторые дешевые лекарства просто исчезли с рынка и находятся в дефектуре, а на смену им пришли более дорогостоящие генерики. В качестве примера можно привести ацикловир. Дешевый препарат за 230 тенге пропал осенью прошлого года, а ему на смену пришли генерики со стоимостью за упаковку от 2 000 до 5000 тенге.
Еще одним примером сокращения ассортимента является ситуация, когда жизненно-важные препараты и препараты экстренной медицины представлены в Государственном реестре и на рынке лишь в одном торговом наименовании от одного единственного производителя. Таким образом, ставится под угрозу его физическая доступность. Примером может служить МНН эпинефрин, который зарегистрирован лишь в одном торговом наименовании украинского производителя. Таким образом мы зависим от этого производителя и при любых нарушениях цепочек поставок препарат может просто исчезнуть с рынка. Между тем, такие лекарства должны быть представлены 2-3 торговыми наименованиями. Недопустимо иметь лишь одно зарегистрированное торговое наименование препарата экстренной помощи от одного производителя, ну, а, если уж такое произошло необходимо контролировать надежность его поставок.
Уже довольно давно в Казахстане было принято решение о поэтапном дерегулировании цен на лекарственные средства. Согласно планам уполномоченного регуляторного органа, к концу этого года в розничном сегменте казахстанского рынка цены на все лекарственные средства будут отпущены. Это крайне важно, поскольку 1 января 2026 года в Казахстане заканчивается целый ряд переходных периодов, в том числе – переход на регистрацию по правилам ЕАЭС, введение обязательного соответствия международному стандарту GPP, а также планируемая налоговая реформа с введением НДС и сменой налоговых режимов. Все эти регуляторные изменения влекут повышение финансовой нагрузки на бизнес, и в этих условиях важно избежать всех возможных рисков для лекарственного обеспечения, и самое главное ухода важных лекарств, которые широко используются в клинической практике и пациентами. Ведь если производители уйдут, они уже не возвратятся. Так как для этого потребуется регистрация по правилам ЕАЭС, которая требует времени и финансовых затрат.

В рамках исполнения Указа Президента Республики Казахстан от 22 июня 2022 г. №938 «Об утверждении Концепции защиты и развития конкуренции в Республике Казахстан на 2022-2026 годы» Агентством по защите и развитию конкуренции Республики Казахстан совместно с Министерством здравоохранения Республики Казахстан была утверждена «Дорожная карта по развитию конкуренции в сфере здравоохранения», в которой было закреплено поэтапное дерегулирование цен на лекарственные средства (далее - ЛС) и вывода из ценового регулирования к 01 января 2026 года всех ЛС, с сохранением ценового регулирования лекарственных средств, приобретаемых в рамках ГОБМП и ОСМС. Указанные в Дорожной карте мероприятия направлены на развитие конкуренции на рынке лекарственного обеспечения путем снижения избыточного ценового регулирования в коммерческом сегменте.
Вместе с тем, 10 апреля 2025 года на интернет-ресурсе «Открытые НПА» был опубликован проект Приказа «О внесении изменений в приказ Министра здравоохранения Республики Казахстан от 11 декабря 2020 года № ҚР ДСМ-247/2020 «Об утверждении правил регулирования, формирования предельных цен и наценки на лекарственные средства, а также медицинские изделия в рамках гарантированного объема бесплатной медицинской помощи и (или) в системе обязательного социального медицинского страхования», которым вносятся изменения, позволяющие экспертной организации производить корректировку цен по уже поданным заявлениям на регистрацию цены по всем ЛС, которые обращаются на фармацевтическом рынке Республике.
Также, до сих пор не вышел очередной приказ «О внесении изменений в приказ исполняющего обязанности Министра здравоохранения Республики Казахстан от 1 декабря 2022 года № ҚР ДСМ-150 «Об утверждении перечня лекарственных средств, подлежащих ценовому регулированию для оптовой и розничной реализации», несмотря на то, что он по законодательству должен быть выпущен не позднее 10 марта текущего года, согласно Кодексу Республики Казахстан «О здоровье народа и системе здравоохранения», проектом которого из перечня ЛС, подлежащих ценовому регулированию для оптовой и розничной реализации были исключены все безрецептурные ЛС.
Таким образом, в настоящее время у фармацевтической отрасли отсутствует подтверждение введения заявленных мер по дерегуляции цен на ЛС в коммерческом сегменте фармацевтического рынка, что может значительно повлиять на оборот ЛС и их доступность для пациентов.
В связи с вышеизложенным возникают вопросы:
- ДОСТИГНУТЫ ЛИ ЦЕЛИ, КОТОРЫЕ ИЗНАЧАЛЬНО ДЕКЛАРИРОВАЛИСЬ ПРИ ВВЕДЕНИИ РЕГУЛИРОВАНИЯ ЦЕН В РОЗНИЧНОМ СЕГМЕНТЕ РЫНКА ОБ ОБЕСПЕЧЕНИИ ЭКОНОМИЧЕСКОЙ ДОСТУПНОСТИ ЛЕКАРСТВ ДЛЯ НАСЕЛЕНИЯ?
- КАК И В КАКИЕ СРОКИ БУДЕТ РЕАЛИЗОВЫВАТЬСЯ ДАЛЬНЕЙШЕЕ ДЕРЕГУЛИРОВАНИЕ ЦЕН НА ЛС В РОЗНИЧНОМ СЕГМЕНТЕ? КОГДА РЫНОК УВИДИТ ПРОЕКТЫ НПА?
- БУДЕТ ЛИ ВВЕДЕН НДС С УЧЕТОМ СИТУАЦИИ С ДОСТУПНОСТЬЮ ЛС?
В заключении спикер отметила, что все вышеизложенное следует расценивать как официальный запрос в адрес регуляторного органа и попросила ответить Министерство здравоохранения РК на поставленные вопросы в установленные законодательством сроки.
Итак, физическая и экономическая доступность лекарственных средств - это комплексная проблема, требующая системного подхода и координации различных государственных и частных структур. Только совместными усилиями можно обеспечить доступ к необходимым медикаментам для всех слоев населения и улучшить качество здравоохранения.
Подготовила Ольга Баимбетова.

В Астане 23-26 апреля 2025 года прошла IV Международная научно-практическая конференция по оценке технологий здравоохранения. В рамках мероприятия ведущие эксперты, представители государственных органов, фармацевтических компаний, производителей медицинских технологий, исследовательских организаций и медицинского сообщества обсудили широчайший спектр вопросов по дальнейшему формированию и развитию системы здравоохранения Казахстана и региона.
 В ходе конференции Вице-Министр здравоохранения Казахстана Ержан Нурлыбаев сообщил, что сегодня перед Министерством здравоохранения РК стоит амбициозная, но четкая задача - создать систему, в которой каждый вложенный ресурс будет ориентирован на пациента, каждое решение - на здоровье, а каждый механизм – на долгосрочный результат. Крайне важно сформировать такую кадровую и лекарственную политику, которая будет не реактивной, а опережающей.
В ходе конференции Вице-Министр здравоохранения Казахстана Ержан Нурлыбаев сообщил, что сегодня перед Министерством здравоохранения РК стоит амбициозная, но четкая задача - создать систему, в которой каждый вложенный ресурс будет ориентирован на пациента, каждое решение - на здоровье, а каждый механизм – на долгосрочный результат. Крайне важно сформировать такую кадровую и лекарственную политику, которая будет не реактивной, а опережающей.
Говоря о развитии фармацевтической отрасли, Ержан Нурлыбаев напомнил, что Главой государства поставлена задача довести долю продукции отечественного производства в общем объеме рынка до 50%. В связи с этим, Министерством здравоохранения РК вносятся изменения в законодательство, направленные на создание благоприятных для этого условий.
Вице-Министр здравоохранения анонсировал выход приказа, объединяющего 12 нормативных документов, регламентирующих регистрацию и обращение лекарственных средств и медицинских изделий на рынке. В соответствии с данным приказом, срок регистрации будет составлять не более 100 дней, а для производителей из стран с сильной регуляторной системой – 15 рабочих дней. При этом услуги, связанные с выводом препарата на рынок, будут оказываться по принципу Единого окна. Основой посыл – сделать рынок интересным для инвесторов и доступным для вывода качественных современных препаратов.

Компания SANTO Member of Polpharma Group официально подтвердила успешное прохождение Европейского аудита на соответствие стандартам Надлежащей производственной практики (GMP) Европейского Союза. Получение сертификата стало важной вехой в развитии компании и открыло новые перспективы для выхода на международные рынки.
В честь этого значимого события 24 апреля 2025 года на территории завода прошла пресс-конференция с участием руководства компании, и представителей СМИ. В рамках мероприятия были освещены ключевые аспекты подготовки к сертификации, значимость стандарта GMP для фармацевтической и производственной отраслей, а также планы компании на будущее.
После официальной части участники мероприятия отправились на экскурсию по цеху по производству твердых пероральных лекарственных средств №3, где внедрены и успешно функционируют стандарты GMP ЕС, а также посетили Центр инноваций и качества SANTO, который включает в себя лабораторию контроля качества, микробиологическую лабораторию и научно-исследовательский и инновационный центр (НИИЦ) компании, чтобы лично увидеть современные лаборатории, оборудование и разработки в действии.
«Для нас, как флагмана отечественной фармацевтической отрасли, главным приоритетом является обеспечение пациентов Казахстана доступными качественными лекарственными средствами и дальнейшее укрепление национальной лекарственной безопасности по всем критически важным основным лекарственным средствам. Этот успех - не только большое достижение для компании, но и настоящий прорыв в истории отечественной фарм. индустрии Казахстана, поскольку подобный сертификат является единственным среди фарм. производителей во всей Центральной Азии.
Всё это позволяет нам выйти на широкий спектр международных рынков, включая Европу, США и Ближний Восток. Важным элементом сертификации по стандартам GMP ЕС стало открытие нашего нового Центра инноваций и качества с современным лабораторным комплексом стоимостью около 20 млн евро», — отметил Адам Алексеюк, генеральный директор SANTO.
Сертификация GMP ЕС стала возможной благодаря системной работе всей команды, модернизации производства, внедрению цифровых решений и выстраиванию культуры качества на всех уровнях.
Справка:
GMP (Good Manufacturing Practice) — международный стандарт, регулирующий производство лекарственных средств, продуктов питания и других чувствительных к качеству товаров. Сертификат GMP ЕС подтверждает, что продукция компании соответствует самым высоким требованиям безопасности, эффективности и стабильности.

Премьер-министр Олжас Бектенов провел заседание Совета по улучшению инвестиционного климата по вопросам развития сферы здравоохранения с участием руководителей посольств США, Европейского союза, Канады, Американской торговой палаты, а также региональными директорами международных компаний, лидеров отрасли, таких как Johnson&Johnson, Pfizer, AstraZeneca, Kazanada LLP, La Roche и др. Об этом сообщается на официальном информационном ресурсе Премьер-министра РК.
«В своем Послании народу Президент Касым-Жомарт Токаев подчеркнул необходимость реализации комплексных мер для укрепления здоровья нации. Учитывая важность данной задачи, Правительством принимаются все меры по совершенствованию системы здравоохранения. Мы нацелены на увеличение объема инвестиций, локализацию производств, создание кластеров высокого передела с участием инвесторов. Убежден, что активное взаимодействие и обмен мнениями в рамках Совета придаст дополнительный импульс нашим совместным усилиям по развитию здравоохранения и росту деловой активности в Казахстане», – отметил Олжас Бектенов.
В РК ведется масштабная модернизация медицинской инфраструктуры с акцентом на укрепление сельской и первичной медико-санитарной помощи. В рамках Национального проекта «Модернизация сельского здравоохранения» построено 467 медицинских объектов в сельских округах. Продолжается последовательная модернизация многопрофильных больниц в районах.
Активно применяются цифровые решения с поэтапной оцифровкой всех процессов, в том числе по амбулаторному лекарственному обеспечению. Внедряется технология искусственного интеллекта для диагностики заболеваний, использования персонализированных AI-ассистентов для врачей и пациентов. Создается Единое хранилище медицинских данных, благодаря чему будет достигнут 100%-ый охват врачебных сведений с контролем их полноты и качества.
Внимание уделено мерам по стимулированию локализации производства фармацевтической продукции. В целях увеличения доли отечественного производства лекарственных средств и медицинских изделий до 50% к 2029 году Правительством усилена работа по улучшению бизнес-климата страны. Законодательством предусмотрены инвестиционные преференции, включая налоговые льготы, натурные гранты, долгосрочные контракты и др. Упрощается законодательство по выходу лекарственных средств на рынок с 2 лет до 100 рабочих дней. Заключено 90 долгосрочных договоров с 34 производителями на производство около 2,5 тыс. наименований фармпродукции. Налажено активное взаимодействие с ведущими мировыми фармацевтическими компаниями, среди которых Pfizer, AstraZeneca, Roche и др. для локализации производства инновационных препаратов, включая трансферт технологий и обучение персонала.
В ходе встречи помимо перспектив привлечения инвестиций в сферу здравоохранения были обсуждены проблемные вопросы и пути их решения в диалоге с бизнесом.
Исполнительный директор Американской торговой палаты в Казахстане Джефф Эрлих отметил имеющийся прогресс Казахстана в сфере здравоохранения. По его словам, за более чем 20 лет, проведенные в стране, он стал свидетелем значительных улучшений, которые положительно отражаются на здоровье нации. Он подчеркнул, что рост показателей здравоохранения сопровождается внедрением новых технологий и качественного оборудования. Джефф Эрлих также акцентировал внимание на важности свободной торговли и подтвердил готовность Торговой палаты США укреплять торговые отношения с Казахстаном.
Временная поверенная в делах США в РК Дебора Робинсон затронула вопросы усиления защиты прав интеллектуальной собственности на лекарственные средства и внедрения регуляторных механизмов, соответствующих международным стандартам и лучшим практикам.
Посол Европейского Союза в РК Алешка Симкич в своей речи отметила положительные результаты сотрудничества между ЕС и Казахстаном в секторе здравоохранения. В частности, высокая оценка дана проекту Евросоюза, реализуемого при поддержке ВОЗ в Казахстане и Центральной Азии, а также взаимодействию через Платформу высокого уровня ЕС-Казахстан и двустороннюю Рабочую группу по вопросам доступа к рынку в сфере здравоохранения и здравоохранительной политики.
Посол Канады в Казахстане и по совместительству в Кыргызстане, Таджикистане, Туркменистане, Узбекистане Кристофер Дагган подчеркнул важность сотрудничества в области развития инновационных технологий для привлечения инвесторов и поддержки талантливых специалистов. В частности, отмечена заинтересованность Канады в стратегическом партнерстве с Казахстаном в области трансформации системы здравоохранения через образование, внедрение передовых технологий и др.
Генеральный директор Johnson & Johnson в Казахстане Адилет Назарбаев актуализировал вопрос доступности онкопрепаратов для пациентов в рамках государственного финансирования. Отмечена важность сокращения периода с момента регистрации до приема лекарства онкобольными до 100 дней – на сегодня Министерством здравоохранения проводится соответствующая работа.
Региональный Директор Pfizer по Казахстану, Центральной Азии, Кавказу и Монголии, член Совета директоров Американской Торговой Палаты Дмитрий Козенков подчеркнул значимость запуска контрактного производства оригинальных запатентованных лекарств в Казахстане как качественного шага в развитии фармпромышленности.
Президент по региону Центральной Азии, GE HealthCare Дмитрий Занчев отметил потенциал Казахстана стать технологическим производственным хабом в регионе. Особое внимание уделено эффективности инструментов привлечения инвестиций.
Директор AstraZeneca Kazakhstan Мария Шипулева выразила поддержку курсу Президента РК на увеличение доли отечественного производства лекарств.
«Мы поддерживаем курс Главы государства по увеличению производства до 50% к 2029 году, а также привлечение международных инвестиции в инновационную фармацевтику. Три инновационные компании, в том числе наша, приняли решение о локализации на казахстанских производственных площадках. Мы уже инвестировали около 5 млн долларов. До 2030 года сумма инвестиций составит около 40 млн долларов. Первая партия товара будет выпущена через месяц», - отметила она.
Директор компании подчеркнула, что такие проекты не только способствуют развитию науки и инновационной диагностики, но и создают высококвалифицированные кадры. По ее словам, международные компании начали более активно инвестировать, увидев поддержку со стороны государства и заинтересованность в инициировании таких проектов.
Генеральный директор Kazanada LLP Кевин Фрик отметил необходимость модернизации системы подготовки специалистов для неотложной медицинской помощи. По его словам, сегодня преподавать такие курсы могут только специалисты с высшим медицинским образованием, что ограничивает возможности. Кевин Фрик предложил разрешить обучение и преподавание фельдшерам и медсестрам, прошедшим профильную подготовку, как это принято в международной практике. Также он подчеркнул важность оснащения колледжей Казахстана международными программами по различным видам экстренной помощи, чтобы выпускники могли эффективно работать в скорой помощи с первого дня.
Озвученные вопросы и предложения прокомментировала министр здравоохранения РК Акмарал Альназарова. Отмечено значительное увеличение объемов амбулаторного обеспечения, которое с 2018 года выросло более чем в 3 раза и достигло 250 млрд тенге. Сегодня Министерством здравоохранения ведется актуализация перечня амбулаторного лекарственного обеспечения с учетом влияния препаратов на смертность, продолжительность жизни и инвалидизацию. Вопросы оцифровки бизнес-процессов и регистрации фармпродукции по принципу «единого окна» будут завершены до 1 июля т.г. Также пересмотрены механизмы ценообразования лекарств, внедрена интеграция информационных систем с базами данных Минфина и таможенных служб, что позволяет обеспечить прозрачность, стабильность цен и стимулирование конкуренции.
По итогам заседания Совета по улучшению инвестиционного климата Премьер-министр поручил Министерству здравоохранения проработать озвученные предложения и рекомендации зарубежных партнеров.
Актуальные интервью

В последние годы наблюдается впечатляющий прогресс в области разработки прорывных терапевтических продуктов для лечения заболеваний, в том числе тех, которые раньше не только не поддавались лечению, но даже не диагностировались. Однако все еще сохраняется важная задача по обеспечению доступа для пациентов к таким передовым препаратам и их выводу на рынок Казахстана. Эти и другие вопросы мы обсудили с управляющим директором Johnson & Johnson Innovative Medicine по региону pазвивающиеся рынки ЕМЕА АСГАРОМ РАНГУНВАЛА.
- Асгар, на позиции управляющего директора по развивающимся рынкам региона ЕМЕА, у Вас есть возможность наблюдать за фармацевтическими рынками разных стран. Какие глобальные тенденции сейчас наблюдаются в разработке инновационных препаратов?
- Развитие науки всегда ориентировано на незакрытые потребности здравоохранения. Если бы вы задали мне этот вопрос два года назад, я бы ответил, что приоритетом исследований и разработок является поиск эффективных методов лечения серьезных жизне-угрожающих заболеваний, таких как рак. В этой области достигнуты значительные успехи, включая инновации в прецизионной и персонализированной медицине, а также в методах иммунной, генной и клеточной терапии.
Сегодня, в 2025 году, мы наблюдаем смещение фокуса с исключительно сложных заболеваний на решение проблем, связанных с образом жизни и внешностью – избыточным весом и ожирением. Конечно, важно учитывать, что избыточный вес и ожирение могут привести к серьезным заболеваниям, а их эффективное лечение играет ключевую роль в профилактике и снижении рисков для здоровья.
Примечательно, что когда речь идет о сохранении жизни, например, при лечении онкологических заболеваний, пациенты зачастую не готовы самостоятельно оплачивать терапию, полагаясь на поддержку государства или страховых систем. Однако в случае решений, связанных с внешностью, люди охотно инвестируют в инновационные препараты.
Этот контраст поднимает важный вопрос доступности передовых медицинских разработок для пациентов.
- Какие же ключевые вызовы в здравоохранении сегодня определяют доступ пациентов к инновационным препаратам?
- Можно выделить два ключевых фактора. Во-первых, сегодня во многих странах Северного полушария, включая Западную Европу, Казахстан, Россию, наблюдается тенденция старения населения, в отличие, к примеру, от государств Африки, где доля молодого населения остается высокой. В нашем регионе увеличивается количество пожилых людей, которые чаще сталкиваются с хроническими и серьезными заболеваниями. Это приводит к росту потребности в длительном и зачастую дорогостоящем лечении, что, в свою очередь, увеличивает нагрузку на системы здравоохранения.
Во-вторых, инновационные лекарства, как правило, имеют высокую стоимость. Так как в их разработку, исследования, производство и организацию доступа на рынок вкладываются значительные финансовые инвестиции. Кроме того, применение этих инновационных лекарств часто сопряжено с необходимостью использования дорогостоящих методов диагностики и специализированных терапевтических подходов.
Таким образом, рост расходов на здравоохранение обусловлен демографическими изменениями и необходимостью внедрения инновационных технологий с высокой клинической ценностью.
- В каждой стране действуют свои подходы к регистрации и возмещению инновационных лекарств для решения этих вызовов. На ваш взгляд, как за последние годы изменились эти процессы на глобальном уровне?
- Государства могут по-разному подходить к вопросу обеспечения доступности инновационных препаратов. В одних странах процесс принятия решений о возмещении может затягиваться, а доступ к препарату ограничивается узким кругом пациентов. В других – акцент делается на снижение стоимости лекарства.
В Казахстане внедрение инновационных препаратов в систему лекарственного обеспечения – длительный и многоэтапный процесс. Для включения лекарства в перечень возмещения требуется пройти строго установленные законодательные процедуры, что может занять несколько лет. Кроме того, имеются ограничения в доступе по каналам возмещения. Например, пациент может получить препарат в стационаре, но на амбулаторном уровне лекарство становится недоступным.
Один из способов оптимизации затрат - регулирование цен на воспроизведенные препараты. Для примера в западных странах 80% финансирования расходуется на покупку препаратов, защищенных патентом, а 20% - на дженерики. Причем, если анализировать закуп в натуральном выражении, то картина будет зеркальной – примерно 80% объема упаковок составят дженерики, а 20% – препараты, находящиеся под патентной охраной.
В Казахстане мы наблюдаем несколько иную пропорцию: в стоимостном объеме закупки доли дженериков и препаратов, находящихся под патентной защитой, почти равны.
- Получается, что на дженерики мы тратим больше денег?
- Приведу пример: в Германии цена на препарат снижается на 90% сразу после окончания срока действия патентной защиты на оригинальный препарат ввиду появления воспроизведенных лекарств. В Казахстане и на других развивающихся рынках этот процесс более длительный и может занимать 2–3 года и более. Причиной этому является поддержка локальных производителей лекарств, что тоже необходимо. Но, если оценивать влияние на ВВП, которое локальные производители оказывают, получая такую поддержку, оно получается не столь значимым.
В этом контексте Министерство здравоохранения Казахстана уже внесло изменения в нормативные акты для более эффективного регулирования данного вопроса. Конечно, впереди еще предстоит работа по приведению цен на воспроизведенные препараты в соответствие с рыночными реалиями, но в итоге это поможет повысить доступность лекарств для пациентов
- Мы знаем, что при поддержке Johnson & Johnson прошло исследование по срокам доступа пациентов к противоопухолевым лекарственным средствам к возмещению в рамках ГОБМП и системе ОСМС. Оно выявило значительные задержки в регистрации и возмещении инновационных препаратов в Казахстане. Как эти данные соотносятся с глобальными тенденциями?
- Основная проблема — значительный разрыв между регистрацией препарата и его включением в систему лекарственного возмещения. В среднем этот период в Казахстане составляет около пяти лет. Это своеобразный антирекорд и один из самых длительных сроков среди всех рынков, с которыми мне доводилось работать.
- К слову, сейчас эта проблема постепенно решается и, может быть, уже к 2026 году некоторые процедуры будут проводиться не последовательно, а параллельно, что ускорит вход препарата в систему ГОБМП и ОСМС. Какие механизмы оптимизации этого процесса можно позаимствовать из международного опыта?
- Во многих развитых странах мира имеются системы оценки технологий здравоохранения. Поэтому Казахстан, выбрав государства с сопоставимой экономикой и показателями ВВП на душу населения, может ориентироваться на их опыт в ценообразовании при анализе клинической ценности инновационного препарата и использовать тот же подход. Таким образом, можно также сократить время, необходимое для ввода препарата в систему лекарственного обеспечения.
Тем более сделать это несложно, так как чаще всего инновационный препарат подается в Казахстан на регистрацию после его одобрения Управлением по контролю за качеством пищевых продуктов и лекарственных средств (FDA) или Европейским медицинским агентством (ЕМА). Процедура регистрации в Казахстане занимает примерно год, за этот период во многих странах препарат уже прошел оценку клинической ценности, и цена на него уже определена. Поэтому, выбрав корзину референтных стран, можно установить усредненную цену. То есть оптимизация процесса может быть достигнута путём использования международного опыта и системы оценки технологий здравоохранения.
- Есть ли страны, которые уже практикуют такой подход?
- Конечно, таких стран много. Это ОАЭ, Саудовская Аравия, Турция и другие. Зачем изобретать велосипед, когда общепризнанные эксперты в своих областях уже изучили и проанализировали все необходимые процессы, приложили свои знания и компетенции и поняли, какая оптимальная цена может быть установлена на препарат.
- Johnson & Johnson активно поддерживает проекты, инициированные пациентскими организациями, как в Казахстане, так и в других странах. Какие ключевые критерии учитываются при выборе проектов для финансирования? Как, на ваш взгляд, меняется влияние пациентских сообществ на политику в сфере здравоохранения в глобальном масштабе?
- Прежде чем оказывать поддержку какой-либо организации, мы проводим комплексную юридическую проверку, включая оценку репутации. Нам важно убедиться, что это надежная и устойчивая организация с историей, которая действительно оказывает поддержку пациентам, а не просто аккумулирует финансовые средства.
Поддержка таких организаций играет ключевую роль в повышении осведомлённости о заболеваниях, улучшении диагностики и доступе к лечению. Пациенты должны участвовать в принятии решений, связанных с терапевтическими опциями и лекарственным возмещением – их голос должен быть слышен на всех этапах, от выявления заболевания до подбора оптимальной терапии. Получение качественного лечения — это законное право каждого гражданина, и именно пациентские организации помогают отстаивать эти права.
Как компания мы поддерживаем пациентские организации, поскольку их мнение действительно важно. Радует, что в Казахстане система здравоохранения стремится учитывать потребности пациентов и готова к открытому диалогу. В конечном итоге, все участники сферы здравоохранения – и фармацевтические компании, и государственные органы, работают ради единой цели — улучшения качества жизни пациентов.
- Какие механизмы взаимодействия с регуляторами наиболее эффективны на глобальном уровне, и как этот опыт можно применить в Казахстане?
- Эффективное взаимодействие с регуляторами строится, прежде всего, на постоянном и открытом диалоге. Например, в США Управление по контролю за качеством пищевых продуктов и лекарственных средств (FDA) предоставляет возможность обсуждать ключевые аспекты разработки лекарств уже на самых ранних стадиях – от механизма действия до планирования клинических испытаний. Подобный подход применяет и Европейское медицинское агентство (EMA), что позволяет обеспечивать контролируемый, устойчивый и безопасный доступ пациентов к инновационным препаратам.
Важно, что правительство Казахстана также демонстрирует готовность к открытому диалогу с представителями отрасли. Мне уже довелось встретиться с министром здравоохранения, и этот опыт подтверждает, что в стране есть стремление к обсуждению ключевых вопросов и поиску решений. Мы также видим, что руководство принимает во внимание дополнительные механизмы расширения доступности к инновационным лекарственным препаратам, которые предлагают компании, и на основании в том числе этих дополнительных возможностей принимает решение о включении тех иных опций в перечни лекарственного возмещения.
- Насколько, на Ваш взгляд, эффективны технологии cost- и risk-sharing в плане обеспечения доступа к инновациям?
- По сути, cost-sharing можно рассматривать как форму скидки, и наша компания всегда готова к открытому обсуждению подобных механизмов. Однако важно понимать, что для действительно инновационных препаратов, которые значительно превосходят существующие стандарты лечения по эффективности, цена всегда будет оставаться премиальной.
Что касается risk-sharing или программ разделения рисков, изначально эта модель воспринималась во всем мире очень позитивно. Однако со временем стало очевидно, что ее реализация требует сложного администрирования, что делает экономический эффект спорным. Для работы программы необходим регистр пациентов, постоянный мониторинг их состояния, а также специалист, который будет обрабатывать и анализировать данные. Кроме того, важно четко определить конечные критерии оценки риска, что усложняется из-за индивидуальных различий между пациентами – образа жизни, сопутствующих факторов и реакции на лечение. В результате затраты на администрирование такой программы зачастую превышают потенциальную экономию для государства.
- Какие выгоды помимо самого препарата, получает государство, пациенты и в целом здравоохранение, когда компания выводит на рынок инновационную технологию?
- Инновационные технологии не только повышают уровень качества оказания медицинских услуг, но и способствуют развитию всей системы здравоохранения. Их внедрение требует обучения врачей, совершенствования диагностики и, в некоторых случаях, даже новых подходов к лечению. Однако главное — инновации способны кардинально изменить терапевтические подходы. Например, один из наших новых препаратов для лечения рака легкого на поздних стадиях позволяет пациентам получить дополнительный год качественной жизни, и такая возможность действительно бесценна.
При этом работа систем здравоохранения в разных странах существенно отличается. В развитых странах, например в Германии, медицинская помощь организована так, что пациент проходит через четкую цепочку специалистов, что позволяет ему не «выпадать» из системы. В развивающихся странах этот процесс может быть менее структурированным: пациенты часто сталкиваются со сложностями с диагностикой, вынуждены обращаться к разным врачам и могут терять драгоценное время.
Мы стремимся поддерживать систему здравоохранения комплексно: помогаем направлять пациентов к профильным специалистам, обучаем врачей, а также реализуем программы по повышению осведомленности о заболеваниях среди пациентов и медицинского сообщества. Такой подход не только улучшает качество диагностики и лечения, но и способствует устойчивому развитию здравоохранения в целом.
- Какие перспективные продукты имеются у компании?
- Как я уже отмечал, у нас есть препарат для лечения рака лёгкого на поздних стадиях, который помогает пациентам продлить жизнь на целый год, сохраняя ее качество. Помимо этого, мы разрабатываем прорывной препарат для лечения язвенного колита и болезни Крона. На подходе инновационная терапия рака мочевого пузыря, представляющая собой уникальное сочетание лекарственного препарата и медицинского устройства — настоящий революционный подход в онкологии.
В Казахстане мы сосредоточены на расширении портфеля препаратов для лечения множественной миеломы, чтобы дать пациентам доступ к современным и эффективным терапевтическим решениям. В целом, Johnson & Johnson предлагает широкий спектр инновационных решений, направленных на улучшение здоровья и качества жизни пациентов.
Мы в Johnson & Johnson стремимся не только разрабатывать инновационные решения, но и поддерживать систему здравоохранения. У Казахстана есть большой потенциал для внедрения передовых технологий в медицине, и мы рады быть частью этого процесса. Надеемся, что совместными усилиями мы сможем сделать качественное лечение доступнее, а систему здравоохранения — более устойчивой и ориентированной на пациента.
- Асгар, спасибо Вам большое за интервью.
Материал подготовила Ольга Баимбетова.

Приказом Министра здравоохранения Республики Казахстан от 16 апреля 2025 года №38 внесены изменения в перечень лекарственных средств и медицинских изделий для бесплатного и (или) льготного амбулаторного обеспечения отдельных категорий граждан Республики Казахстан с определенными заболеваниями (состояниями).
В соответствии с ними:
- из перечня ЛС в рамках ГОБМП перечня исключены препараты для лечения язвенной болезни желудка и 12-перстной кишки омепразол, висмута трикалия дицитрат, амоксициллин, кларитромицин, метронидазол;
- из перечня ЛС в системе ОСМС для взрослых исключены препараты для лечения:
- внебольничной пневмонии легкой и средней степени тяжести - амоксициллин, азитромицин;
- гастроэзофагальной рефлюксной болезни - омепразол, фамотидин;
- поражения черепных нервов - карбамазепин,
- острго/хронического синусита легкой и средней степени тяжести - амоксициллин, азитромицин;
- острого/хронического гнойного среднего отита легкой и средней степени тяжести - амоксициллин, азитромицин;
- острого/ хронического кератита легкой и средней степени тяжести - офлоксацин, тобрамицин, ацикловир;
- острого/хронического блефарита/конъюнктивита/иридоциклита легкой и средней степени тяжести - хлорамфеникол, тобрамицин;
- эритемы многоформной - хлорамфеникол, тобрамицин;
- гиперплазии предстательной железы - доксазозин, дутастерид;
- доброкачественной дисплазии молочной железы - бромокриптин, тамоксифен;
- эндометриоза - диеногест, левоноргестрел.
- хронических инфекций мочеполовой системы легкой и средней степени тяжести - амоксициллин, амоксициллин и клавулановая кислота, цефуроксим, цефиксим, сульфаметоксазол и триметоприм, ципрофлоксацин, нитрофурантоин;
- из перечня ЛС, МИ и специализированных лечебных продуктов в системе ОСМС на амбулаторном уровне для детей до 18 лет исключены препараты для лечения:
- синусита/болезни миндалин и аденоидов - амоксициллин и клавулановая кислота, цефуроксим, азитромицин;
- гастроэзофагеальной рефлюксной болезни - ранитидин, томепразол, эзомепразол, метоклопрамид, домперидон;
- гастрита и дуоденита - ранитидин, томепразол, эзомепразол, метоклопрамид, домперидон, амоксициллин, кларитромицин, метронидазол;
- хронического панкреатита - омепразол, мультиферменты (липаза, протеаза и т.д.), октреотид, ибупрофен, парацетамол;
- холецистита/ холангита - урсодезоксихолевая кислота, амоксициллин, цефуроксим;
- желчекаменной болезни - урсодезоксихолевая кислота;
- мигрени - диклофенак, ибупрофен, парацетамол, суматриптан;
- поражений тройничного нерва - карбамазепин, окскарбазепин;
- гастроэнтерита и колита инфекционного происхождения легкой и средней степени тяжести - глюкоза безводная, натрия хлорид, калия хлорид, натрия цитрат, парацетамол, ибупрофен, ондансетрон, азитромицин;
- ветряной оспе легкой и средней степени тяжести - ацикловир, парацетамол, ибупрофен;
- инфекциях, вызванных вирусом герпеса/ опоясывающего лишая легкой и средней степени тяжести - валацикловир, ацикловир в таблетках и мази, парацетамол, ибупрофен;
- амебиаза, лямблиоза, трихомониаза у детей с легким, средне-тяжелым течением, без осложнений - метронидазол;
- аскаридоз энтеробиоз анкилостомидоз - мебендазол, албендазол, левамизол;
- воспалительных заболеваний органов слуха - амоксициллин и клавулановая кислота, азитромицин, ибупрофен, парацетамол;
- крапивницы и эритемы, ангионевротического отека - метилпреднизолон, преднизолон, хлоропирамин, цетиризин, лоратадин;
- инфекций кожи и подкожной клетчатки - амоксициллин и клавулановая кислота, цефуроксим, азитромицин, ибупрофен, парацетамол;
- острого/хронического тубулоинтерстициального нефрита - амоксициллин и клавулановая кислота, цефуроксим, цефиксим, сульфаметоксазол и триметоприм;
- инфекций мочевыводящих путей цистита уретрита и уретрального синдрома - амоксициллин и клавулановая кислота, сульфаметоксазол и триметоприм, нитрофурантоин;
- инфекций мочеполовых органов - доксициклин, амоксициллин и клавулановая кислота, кларитромицин, азитромицин, метронидазол, флуконазол, ибупрофен.
Как сообщало МЗ РК на этапе обсуждения данного документа, высвобождаемые в результате внесенных изменений финансовые средства будут перенаправлены на обеспечение лекарственными средствами при лечении хронических заболеваний, приводящих к серьезным последствиям, а также несущим финансовое бремя на пациентов и их семьи.
Таким образом, в результате исключения вышеуказанных нозологий в Перечне АЛО остаются хронические заболевания, требующие долгосрочного и более затратного лечения.
Приказ вводится в действие по истечении десяти календарных дней после первого официального опубликования.
Официальное опубликование приказа состоялось 22 апреля 2025 года.
Программа автоматизации для аптек Казахстана
Новости
Правила формирования перечня недобросовестных поставщиков лекарств утратили силу

ВОЗ опубликован отчет об использовании антибиотиков в 2022 году. Лидером стал амоксициллин

Краткая информация о системах регулирования цен на лекарственные средства в государствах-членах ЕАЭС

Созданы «умные» стельки, которые помогают в диагностике и лечении целого ряда заболеваний

В Казахстане изменились правила проведения мероприятий по профилактике туберкулеза

В РК утверждены квоты на наркотические средства, психотропные вещества и прекурсоры

Закон по вопросам определения страны происхождения товаров одобрен Сенатом Парламента РК

МЗ РК расширен перечень видов деятельности, выполняемых субъектами госмонополии

В Мажилисе озвучены проблемы фармпроизводителей, связанные с включением в закупочные перечни
Статьи
В Алматы прошли уникальные высокотехнологичные опе...

В РК начинается пилотный проект по регистрации ЛС ...

Фармацевтический рынок Казахстана: вызовы и риски ...

Казахстан упрощает регистрацию и обращение лекарст...

SANTO Member of Polpharma Group получила сертифика...

В Правительстве РК прошло заседание по вопросам ра...
Глобальные тенденции развития фармрынка и проблемы...
В Казахстане внесены изменения в перечень бесплатн...

Между КазНМУ им. С.Д. Асфендиярова и Альянсом инно...

Здравоохранение Республики Казахстан: современное ...
Аналитика

Медицинский представитель - работа мечты или време...
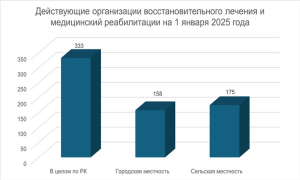
В Казахстане функционирует 333 санаторно-курортных...

Промоция и назначения на фармацевтическом рынке Ка...
Сколько казахстанцы тратят на платные медицинские ...

В Казахстане сетевые аптеки аккумулируют львиную д...

Фармацевтический рынок Республики Казахстан: обзор...
Анализ состояния конкуренции на рынке оптовой реал...
В 2024 году объем производства фармацевтической пр...

В III квартале 2024 года организациями здравоохран...


 English
English العربية
العربية 简体中文
简体中文 Français
Français Русский
Русский Español
Español Қазақ тілі
Қазақ тілі